Rezdiffra (resmetirom) ໄດ້ຮັບການອະນຸມັດໂດຍ FDA ຂອງສະຫະລັດອາເມລິກາສໍາລັບການປິ່ນປົວຜູ້ໃຫຍ່ທີ່ມີ steatohepatitis noncirrhotic ທີ່ບໍ່ມີເຫຼົ້າ (NASH) ທີ່ມີຮອຍແປ້ວຕັບປານກາງເຖິງກ້າວຫນ້າ (fibrosis), ເພື່ອນໍາໃຊ້ພ້ອມກັບອາຫານແລະການອອກກໍາລັງກາຍ.
ຈົນກ່ວາໃນປັດຈຸບັນ, ຄົນເຈັບທີ່ມີ steatohepatitis noncirrhotic ທີ່ບໍ່ມີເຫຼົ້າ (NASH) ທີ່ມີຮອຍແປ້ວຕັບທີ່ໂດດເດັ່ນຍັງບໍ່ມີຢາທີ່ສາມາດແກ້ໄຂໄດ້ໂດຍກົງ. ຄວາມເສຍຫາຍຕັບ. FDA ຂອງ ການອະນຸມັດຂອງ Rezdiffra ຈະ, ເປັນຄັ້ງທໍາອິດ, ສະຫນອງການ ການປິ່ນປົວ ທາງເລືອກສໍາລັບຄົນເຈັບເຫຼົ່ານີ້, ນອກເຫນືອໄປຈາກອາຫານແລະການອອກກໍາລັງກາຍ.
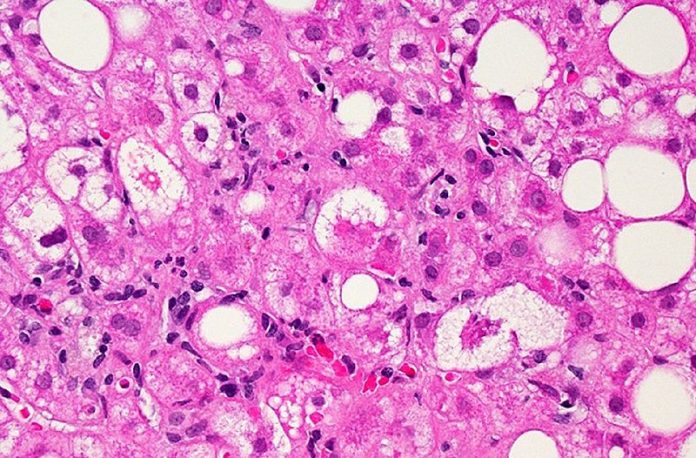
NASH ແມ່ນຜົນມາຈາກການກ້າວຫນ້າຂອງໄຂມັນທີ່ບໍ່ມີເຫຼົ້າ ຕັບ ພະຍາດ ບ່ອນທີ່ ຕັບ ການອັກເສບ, ເມື່ອເວລາຜ່ານໄປ, ສາມາດເຮັດໃຫ້ເກີດຮອຍແປ້ວຂອງຕັບແລະຄວາມຜິດປົກກະຕິຂອງຕັບ. NASH ມັກຈະກ່ຽວຂ້ອງກັບບັນຫາສຸຂະພາບອື່ນໆເຊັ່ນ: ຄວາມດັນເລືອດສູງແລະພະຍາດເບົາຫວານປະເພດ 2. ໂດຍການຄາດຄະເນຢ່າງຫນ້ອຍຫນຶ່ງ, ປະມານ 6-8 ລ້ານຄົນໃນສະຫະລັດມີ NASH ທີ່ມີຮອຍແປ້ວຕັບໃນລະດັບປານກາງເຖິງກ້າວຫນ້າ, ດ້ວຍຕົວເລກດັ່ງກ່າວຄາດວ່າຈະເພີ່ມຂຶ້ນ.
Rezdiffra ເປັນຕົວກະຕຸ້ນບາງສ່ວນຂອງ receptor ຮໍໂມນ thyroid; ການກະຕຸ້ນຂອງ receptor ນີ້ໂດຍ Rezdiffra ໃນຕັບຫຼຸດຜ່ອນການສະສົມໄຂມັນຕັບ.
ຄວາມປອດໄພແລະປະສິດທິພາບຂອງ Rezdiffra
ຄວາມປອດໄພແລະປະສິດທິພາບຂອງ Rezdiffra ໄດ້ຖືກປະເມີນໂດຍອີງໃສ່ການວິເຄາະຈຸດສິ້ນສຸດຂອງຕົວແທນໃນເດືອນ 12 ໃນ 54 ເດືອນ, ແບບສຸ່ມ, double-blind ການທົດລອງ placebo-blind. ຈຸດສິ້ນສຸດຕົວແທນໄດ້ວັດແທກຂອບເຂດຂອງ ຕັບ ການອັກເສບແລະຮອຍແປ້ວ. ຜູ້ສະຫນັບສະຫນູນແມ່ນຈໍາເປັນຕ້ອງໄດ້ດໍາເນີນການສຶກສາຫຼັງການອະນຸມັດເພື່ອກວດສອບແລະອະທິບາຍຜົນປະໂຫຍດທາງດ້ານຄລີນິກຂອງ Rezdiffra, ເຊິ່ງຈະເຮັດໄດ້ໂດຍຜ່ານການສໍາເລັດການສຶກສາ 54 ເດືອນດຽວກັນ, ເຊິ່ງຍັງດໍາເນີນຕໍ່ໄປ. ເພື່ອລົງທະບຽນໃນການທົດລອງ, ຄົນເຈັບຈໍາເປັນຕ້ອງມີ a ຕັບ biopsy ສະແດງໃຫ້ເຫັນການອັກເສບເນື່ອງຈາກ NASH ທີ່ມີລະດັບປານກາງຫຼືກ້າວຫນ້າ ຕັບ ຮອຍແປ້ວ. ໃນການທົດລອງ, 888 ວິຊາໄດ້ຖືກມອບຫມາຍແບບສຸ່ມທີ່ຈະໄດ້ຮັບຫນຶ່ງໃນດັ່ງຕໍ່ໄປນີ້: placebo (294 ວິຊາ); 80 ມິນລີກຣາມຂອງ Rezdiffra (298 ວິຊາ); ຫຼື 100 milligrams ຂອງ Rezdiffra (296 ວິຊາ); ຫນຶ່ງຄັ້ງຕໍ່ມື້, ນອກເຫນືອຈາກການດູແລມາດຕະຖານສໍາລັບ NASH, ເຊິ່ງລວມມີການໃຫ້ຄໍາປຶກສາສໍາລັບອາຫານສຸຂະພາບແລະການອອກກໍາລັງກາຍ.
ໃນເວລາ 12 ເດືອນ, ການກວດເລືອດໃນຕັບໄດ້ສະແດງໃຫ້ເຫັນວ່າອັດຕາສ່ວນຫຼາຍຂອງວິຊາທີ່ໄດ້ຮັບການປິ່ນປົວດ້ວຍ Rezdiffra ບັນລຸຄວາມລະອຽດຂອງ NASH ຫຼືການປັບປຸງຮອຍແປ້ວຂອງຕັບເມື່ອທຽບກັບຜູ້ທີ່ໄດ້ຮັບ placebo. ຈໍານວນທັງຫມົດ 26% ຫາ 27% ຂອງວິຊາທີ່ໄດ້ຮັບ 80 ມິນລິກຣາມຂອງ Rezdiffra ແລະ 24% ຫາ 36% ຂອງວິຊາທີ່ໄດ້ຮັບ 100 ມິນລີກຣາມຂອງ Rezdiffra ມີປະສົບການກັບຄວາມລະອຽດຂອງ NASH ແລະບໍ່ມີອາການຮ້າຍແຮງຂຶ້ນຂອງບາດແຜຕັບ, ເມື່ອທຽບກັບ 9% ຫາ 13% ຂອງຜູ້ທີ່ໄດ້ຮັບ. ໄດ້ຮັບ placebo ແລະການໃຫ້ຄໍາປຶກສາກ່ຽວກັບອາຫານແລະການອອກກໍາລັງກາຍ. ລະດັບການຕອບສະ ໜອງ ສະທ້ອນເຖິງການອ່ານຂອງນັກຊ່ຽວຊານດ້ານພະຍາດ. ນອກຈາກນັ້ນ, ຈໍານວນທັງຫມົດ 23% ຂອງວິຊາທີ່ໄດ້ຮັບ 80 ມິນລິກຣາມຂອງ Rezdiffra ແລະ 24% ຫາ 28% ຂອງວິຊາທີ່ໄດ້ຮັບ 100 ມິນລິກຣາມຂອງ Rezdiffra ປະສົບກັບການປັບປຸງໃນ. ຕັບ ຮອຍແປ້ວແລະບໍ່ມີອາການຮ້າຍແຮງຂຶ້ນຂອງ NASH, ເມື່ອທຽບກັບ 13% ຫາ 15% ຂອງຜູ້ທີ່ໄດ້ຮັບ placebo, ຂຶ້ນກັບການອ່ານຂອງແຕ່ລະ pathologist. ສະແດງໃຫ້ເຫັນການປ່ຽນແປງເຫຼົ່ານີ້ໃນອັດຕາສ່ວນຂອງຄົນເຈັບຫຼັງຈາກການປິ່ນປົວພຽງແຕ່ຫນຶ່ງປີແມ່ນສັງເກດເຫັນ, ເປັນ ພະຍາດ ໂດຍທົ່ວໄປແລ້ວມີຄວາມຄືບໜ້າຊ້າໆ ໂດຍຄົນເຈັບສ່ວນໃຫຍ່ໃຊ້ເວລາຫຼາຍປີ ຫຼືຫຼາຍສິບປີເພື່ອສະແດງໃຫ້ເຫັນຄວາມຄືບໜ້າ.
ຜົນຂ້າງຄຽງຂອງ Rezdiffra
ຜົນຂ້າງຄຽງທີ່ພົບເລື້ອຍທີ່ສຸດຂອງ Rezdiffra ລວມທັງການຖອກທ້ອງແລະປວດຮາກ. Rezdiffra ມາພ້ອມກັບຄໍາເຕືອນແລະຂໍ້ຄວນລະວັງບາງຢ່າງເຊັ່ນ: ພິດຕັບຍ້ອນຢາເສບຕິດແລະຜົນຂ້າງຄຽງທີ່ກ່ຽວຂ້ອງກັບຕ່ອມຂົມ.
ຄວນຫຼີກລ່ຽງການໃຊ້ຢາ Rezdiffra ໃນຄົນເຈັບທີ່ເປັນພະຍາດຕັບແຂງ decompensated. ຄົນເຈັບຄວນຢຸດເຊົາການໃຊ້ Rezdiffra ຖ້າພວກເຂົາມີອາການຫຼືອາການຂອງຄວາມຮ້າຍແຮງຂຶ້ນ ຕັບ ເຮັດວຽກໃນຂະນະທີ່ການປິ່ນປົວ Rezdiffra.
ປະຕິສໍາພັນຂອງຢາເສບຕິດ Rezdiffra
ການໃຊ້ Rezdiffra ໃນເວລາດຽວກັນກັບຢາອື່ນໆບາງຊະນິດ, ໂດຍສະເພາະຢາ statins ສໍາລັບການຫຼຸດລົງຂອງ cholesterol, ອາດຈະສົ່ງຜົນໃຫ້ເກີດປະຕິສໍາພັນກັບຢາທີ່ສໍາຄັນ. ຜູ້ໃຫ້ບໍລິການດ້ານສຸຂະພາບຄວນອ້າງອີງໃສ່ຂໍ້ມູນການສັ່ງຢາຢ່າງເຕັມທີ່ສໍາລັບຂໍ້ມູນເພີ່ມເຕີມກ່ຽວກັບປະຕິສໍາພັນຂອງຢາທີ່ມີທ່າແຮງເຫຼົ່ານີ້ກັບ Rezdiffra, ປະລິມານທີ່ແນະນໍາແລະການດັດແກ້ການບໍລິຫານ.
ໄດ້ ອາຫານແລະຢາ ໄດ້ຮັບການອະນຸມັດ Rezdiffra ພາຍໃຕ້ເສັ້ນທາງການອະນຸມັດທີ່ເລັ່ງລັດ, ເຊິ່ງອະນຸຍາດໃຫ້ມີການອະນຸມັດກ່ອນຫນ້າຂອງຢາທີ່ປິ່ນປົວພະຍາດທີ່ຮ້າຍແຮງແລະແກ້ໄຂຄວາມຕ້ອງການທາງການແພດທີ່ບໍ່ມີເງື່ອນໄຂ, ໂດຍອີງໃສ່ຈຸດສຸດທ້າຍທາງດ້ານການຊ່ວຍຕົວແທນຫຼືລະດັບປານກາງທີ່ສົມເຫດສົມຜົນທີ່ຈະຄາດຄະເນຜົນປະໂຫຍດທາງດ້ານຄລີນິກ. ການສຶກສາ 54 ເດືອນທີ່ໄດ້ກ່າວມາຂ້າງເທິງ, ເຊິ່ງກໍາລັງດໍາເນີນຢູ່, ຈະປະເມີນຜົນປະໂຫຍດທາງດ້ານຄລີນິກຫຼັງຈາກການປິ່ນປົວ Rezdiffra 54 ເດືອນ.
Rezdiffra ໄດ້ຮັບການປິ່ນປົວດ້ວຍ Breakthrough, Fast Track ແລະການທົບທວນບູລິມະສິດການອອກແບບສໍາລັບການຊີ້ບອກນີ້.
ໄດ້ ອາຫານແລະຢາ ໄດ້ໃຫ້ການອະນຸມັດຂອງ Rezdiffra ກັບ Madrigal Pharmaceuticals.
***
ທີ່ມາ:
FDA 2024. ການປ່ອຍຂ່າວ – FDA ອະນຸມັດການປິ່ນປົວຄັ້ງທໍາອິດສໍາລັບຄົນເຈັບທີ່ມີບາດແຜຕັບເນື່ອງຈາກພະຍາດຕັບໄຂມັນ. ຂຽນເມື່ອວັນທີ 14 ມີນາ 2024. ມີຢູ່ https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***